请选择
2NaOH+Cl2==NaClO+NaCl+H2O2ΝaΟΗ+Cl2=ΝaClΟ+ΝaCl+Η2Ο其中生成的次氯酸钠(NaClO)易溶于水,为“84”消毒液的有效成分。现向某100 g氢氧化钠溶液中通入一定量氯气,使之与氢氧化钠恰好完全反应,反应后的溶液质量为107.1 g。

初三化学压轴题典型
(2020年孝感)氯气可与氢氧化钠溶液反应,其反应的化学方程式为
2NaOH+Cl2==NaClO+NaCl+H2O2ΝaΟΗ+Cl2=ΝaClΟ+ΝaCl+Η2Ο
其中生成的次氯酸钠(NaClO)易溶于水,为“84”消毒液的有效成分。现向某100 g氢氧化钠溶液中通入一定量氯气,使之与氢氧化钠恰好完全反应,反应后的溶液质量为107.1 g。
(1)参加反应的氯气质量为__g。
(2)反应生成次氯酸钠的质量(请写出计算过程)。
解析通读题目。依据质量守恒定律,化学反应前后物质的总质量不变,因此参加反应的氯气的质量:107.1 g-100 g=7.1 g。根据氯气质量,结合化学方程式可求出生成的次氯酸钠质量为7.45 g。
初三化学经典例题
I.以黄铁矿(主要成分为FeS2)为原料生产硫酸的原理及工艺流程可简示如下: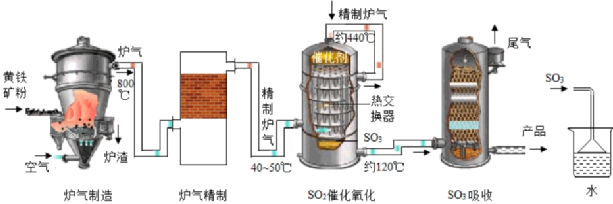
(工艺流程)
(1)黄铁矿是_____(填“纯净物”或“混合物”)工业生产过程中将矿石粉碎的目的是_____。
(2)在吸收装置中,液体由上而下形成喷雾状的目的是_____。
(3)在实验室模拟制硫酸时用如图装置吸收三氧化硫,除了达到与工业上相同的目的外,还可能考虑的因素是_____。
(4)工业上常用石灰乳来吸收尾气中的二氧化硫,请写出反应的化学方程式_____。(提示:生成物有一种是CaSO3)
II.黄铁矿锻烧后的另一种产物是铁的一种氧化物,其中铁氧质量比为7:3,则其化学式为_____。该物质可用来生产氯化铁晶体。氯化铁也是常用的净水剂之一,相比于明矾,其作为净水剂的优点是_____。
III.实验室中常用浓硫酸来配制稀硫酸。实验室用密度为1.84g/cm3、溶质质量分数为98%的浓硫酸来配制500g 20%,需要水_____g.溶解时,应_____,并用玻璃棒不断搅拌。该实验中还需用到的玻璃仪器有烧杯、量筒、_____。请写出稀硫酸的一种用途_____。
IV.某化工厂以黄铁矿为原料产生硫酸。如果该厂生产98%的浓硫酸100t,不考虑其他各生产阶段的物料损失,需要含FeS260%的矿石质量为多少吨?(写出计算过程)________________
【答案】混合物加快反应速率增大反应物的接触面积三氧化硫易溶于水Ca(OH)2+SO2=CaSO3+H2OFe2O3,补充人体需要的铁元素398将浓硫酸盐烧杯壁慢慢注入水中玻璃棒金属除锈100t