请选择
各位同学在查看时请点击全屏查看
2018年吕梁中考化学复习题
(答题时间:90分钟)
(可能用到的原子量:H:1 O:16 C:12 N:14 S:32 Cl:35.5 Fe:56 Na:23 Mg:24 Al:27 Cu:64 Ag:108)
一. 选择题(每小题只有一个选项符合题意)
1. 医疗上抢救危重病人常用的一种气体是( )
A. 氧气 B. 氮气 C. 氢气 D. 二氧化碳
2. 生活中常见的下列现象,属于化学变化的是( )
A. 冰棒融化 B. 米饭变馊
C. 瓷碗破碎 D. 湿衣晾干
日常生活中,我们经常饮用矿泉水,下图是某饮用矿泉水部分商标图,图中列出了理化指标。据此回答3~4题。
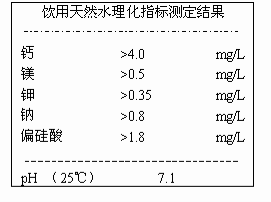
3. 这里的钙、镁、钾、钠指的是( )
A. 单质 B. 原子 C. 分子 D. 元素
4. 这种饮用天然水是( )
A. 酸性 B. 碱性 C. 中性 D. 无法确定
5. 下列离子结构示意图中表示阳离子的是( )
A. 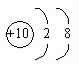 B.
B. 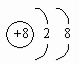
C. 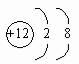 D.
D. 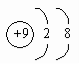
6. 2003年10月15日,我国用“长征”1号F捆绑式火箭将“神舟”五号载人飞船成功送上太空。火箭用联氢(![]() )作燃料,一氧化氮作氧化剂。反应的化学方程式是:
)作燃料,一氧化氮作氧化剂。反应的化学方程式是:![]() 。则X化学式为( )
。则X化学式为( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
7. 区分日常生活中的下列各组物质,所加试剂或操作方法完全正确的是( )
选项 | 需区分的物质 | 操作方法或所加试剂 |
A | 白酒与白醋 | ①观察颜色②闻气味 |
B | 食盐与白糖 | ①稀盐酸②加水溶解 |
C | 合成纤维与天然纤维 | ①烧同时闻气味②观察色泽 |
D | 厕所清洁剂和厨房清洁剂 | ①测pH②石灰石 |
8. 元素符号周围数字有不同的含义,下列符号只表示“2个氢原子”的是( )
A. 2H2 B. H2 C. 2H D. 2H+
9. 小红同学在家做“粗盐的提纯”实验,对其做法的认识中错误的是( )
A. 将粗盐放入玻璃杯中加水溶解::粒子在不断运动
B. 溶解时用筷子搅拌::加快溶解速度
C. 用自制净水器过滤粗盐水::可将粗盐水变为纯净物
D. 实验时不用一次性塑料杯或纸杯::保护环境要从身边小事做起
10. 小玲同学对所学部分化学知识归纳如下,其中有错误的一组是( )

11. 一种新兴的金属由于其密度小、延展性好、耐腐蚀性强,它和它的合金在航空、航海和化学工业中正逐步取代铝和铝的合金而被广泛应用,该金属是()
A. 铜 B. 锌 C. 钛 D. 锰
12. “垃圾是放错了位置的资源”,应该分类回收。生活中废弃的铁锅、铝制易拉罐、铜导线可以归为一类加以回收,因为它们属于()
A. 氧化物 B. 化合物 C. 混合物 D. 金属或合金
13. 我们常说“真金不怕火炼”的原因是( )
A. 金的熔点高 B. 金的硬度大
C. 金的密度大 D. 金不活泼,高温时也不与氧气反应
14. 相同质量的镁和铝分别与足量的稀盐酸充分反应,其结果是( )
A. 镁反应生成的氢气的质量大
B. 铝反应生成的氢气的质量大
C. 铝和镁反应生成的氢气一样多
D. 无法比较生成氢气的质量
15. 为验证铁、铜、铝三种金属的活动性顺序,可选用的一组物质是( )
A. ![]() 溶液、
溶液、![]() 溶液
溶液
B. ![]() 溶液、
溶液、![]() 、
、![]() 溶液
溶液
C. ![]() 溶液、
溶液、![]()
D. ![]() 溶液、
溶液、![]()
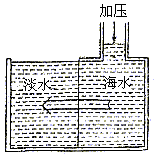
16. 海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡化池,而海水中的各种离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是()
A. 溶质的质量增加 B. 溶剂的质量减少
C. 溶液的质量不变 D. 以上三种情况都有可能
17. 做馒头的面团发酵过度会变酸,要除去酸味,可在面团中加入( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
18. 一木块漂于水中,如图所示,若向水中加入食盐,则木块将( )
A. 上浮 B. 下沉 C. 不变 D. 无法判断

19. 配制100 g 10%的![]() 溶液,用量筒量取水时俯视刻度线,则配制溶液的溶质的质量分数()
溶液,用量筒量取水时俯视刻度线,则配制溶液的溶质的质量分数()
A. 等于10% B. 大于10%
C. 小于10% D. 无法确定
20. 下列物质各5g,在室温下放入100g水中,充分搅拌后,所得溶液的溶质质量分数最小的是( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
21. 下列气体中,既能用浓硫酸干燥,也可以用氢氧化钠干燥的是( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
22. 有些食物的近似pH如下:番茄4.0~4.4,苹果2.9~3.3,柑橘3.0~4.0,鸡蛋清7.6~8.0,当人体胃酸过多时,适合食用的食品是()
A. 番茄 B. 苹果 C. 柑橘 D. 鸡蛋清
23. 人的胃液里含有适量盐酸,可以帮助消化,胃酸过多,反而造成消化不良。下列物质可用来制造治疗胃酸过多的药物的是()
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
24. 检验某溶液是否是酸时,不能选用的试剂是( )
A. 无色酚酞试液 B. 紫色石蕊试液
C. 碳酸钠溶液 D. 锌粒
25. 有关下列物质的用途不正确的是( )
A. 建筑业上利用熟石灰制三合土或砌砖、抹墙
B. 氢氧化钠可用于制肥皂和造纸业
C. 利用硫酸溶液来干燥氢气
D. 利用盐酸除去金属表面的锈
26. 在我国某地曾发生把白色的工业用盐误作食盐的中毒事件,这种工业用盐可能含有( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
27. 玻璃棒不可用来( )
A. 蘸取溶液测定其酸碱度
B. 过滤时引流液体注入漏斗
C. 搅拌漏斗中的悬浊液,加快过滤速度
D. 搅拌烧杯中的溶液,加速溶解
28. 草木灰的主要成分是![]() ,某同学为检验其含有的
,某同学为检验其含有的![]() ,所选择的试剂是( )
,所选择的试剂是( )
A. 澄清的石灰水 B. 水
C. 稀盐酸和澄清的石灰水 D. 稀盐酸
29. 下列几组物质中,按酸、碱、盐顺序排列的是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
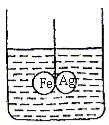
30. 如下图所示的装置,在盛有水的烧杯中,等质量的铁圈和银圈的连接处吊着一根绝缘的细线,使之平衡,小心地从烧杯中央滴入![]() 溶液,观察到的现象是( )
溶液,观察到的现象是( )
A. 铁圈和银圈左右摇摆不定 B. 保持平衡
C. 铁圈向下倾斜 D. 银圈向下倾斜
二. 我会填空
31. 2004年春,轰动全国的安徽阜阳市劣质奶粉事件,导致出现200名“大头婴儿”和10多名婴儿夭亡。经检测,劣质奶粉几乎不含 1 等促进婴儿生长发育的营养素。
32. 医生给病人输液时,常用葡萄糖注射液。下图为葡萄糖注射液的部分标签图,根据下图回答下列问题:

(1)葡萄糖的化学式为![]() ,它是由 2 种元素组成,其相对分子质量是 3 。
,它是由 2 种元素组成,其相对分子质量是 3 。
(2)每克葡萄糖完全氧化约放出17.2 kJ的能量,一瓶这样的葡萄糖注射液可放出 4 kJ的能量。
(3)现要配制10 Kg这种葡萄糖注射液,需用葡萄糖 5 Kg。
33. 最近中国科技大学陈乾旺教授领导的研究组以二氧化碳和金属钠作原料,在440℃和800 atm的条件下,成功合成了金刚石,同时生成氧化钠,首次实现了从二氧化碳到金刚石的逆转变。该反应的化学方程式是 6 ,反应类型是 7 。
34. 2004年4月16日,重庆天原化工厂发生氯气泄漏,事故现场出现大量白雾,给环境造成严重污染。氯气是一种黄绿色并有强烈刺激性气味的有毒气体,可与水反应,化学方程式为:![]() (次氯酸)。
(次氯酸)。
(1)![]() 中氯元素的化合价是 8 。事故现场产生白雾的原因是 9 。
中氯元素的化合价是 8 。事故现场产生白雾的原因是 9 。
(2)消防官兵抢险时,配戴的防毒面具中装有活性炭,其作用是 10 。他们喷洒大量的某种溶液来消除或减轻污染,这种溶液最好是 11 。
35. 今天又是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究:
(1)①此气体是什么物质?验证它的实验方案如下:
猜想 | 实验步骤 | 现象及结论 |
此气体可能是 12 | 13 | 14 |
产生此气体的化学方程式可能是 15 。
②我想制取该气体,采用的发生装置可选取下图中的 16 (填序号),收集装置是 17 。
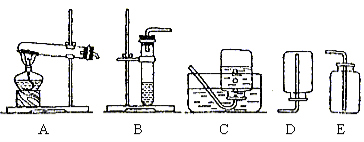
③如用下图装置收集该气体,气体由 18 端(填“a”或“b”)导入。
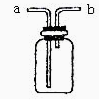
(2)我猜想此无色气体还可能是另外一种气体,可以产生它的化学方程式是 19 。
36. 由于铝元素对人体健康有害,治疗胃酸过多的含铝止酸剂正被新药“胃舒乳”(主要成分是氢氧化镁)所代替,则服用“胃舒乳”治疗胃酸的化学方程式是 20 。
37. 酸、碱、盐溶解性表是学习化学的重要工具。下表列出了“部分酸、碱、盐在20℃时的溶解性”。我能利用此表完成以下任务:
|
|
|
|
|
|
| : | 溶、挥 | 溶、挥 | 溶、挥 | 溶 |
| 溶 | 溶 | 溶 | 溶 | 溶 |
| 微 | 溶 | 溶 | 不 | 微 |
| 溶 | 溶 | 溶 | 不 | 不 |
| 不 | 溶 | 溶 | 不 | 溶 |
(1)查:![]() 的溶解性 21 。
的溶解性 21 。
(2)写化学式:一种酸 22 ;一种不溶于水的盐 23 。
(3)判断:氯化钠溶液与硝酸钙溶液能否发生反应及其理由是 24 。
(4)写化学方程式:铁或铝与表中的一种盐反应 25 。
38. 对知识的归纳与整理是学习化学的一种重要方法。现有三个化学反应如下:
①![]() ②
②![]() ③
③![]()
(1)通过比较我发现:它们有许多相似之处,其一 26 ,其二 27 ……我能另写一个符合这两点的化学方程式 28 ;它们之间也存在相异之处,其中一个反应与众不同,这个反应和它的不同之处是 29 。
(2)课外学习![]() 后,我又发现它也和上述三个反应相似,其相似之处是 30 。
后,我又发现它也和上述三个反应相似,其相似之处是 30 。
三. 我会设计
39. 我到外婆家去作客,见外公购回了一袋碳铵(化学式是![]() )化肥,印在包装袋上的部分说明如下图所示,对此,我有许多问题要探究:
)化肥,印在包装袋上的部分说明如下图所示,对此,我有许多问题要探究:

我探究的问题 | 我的解答 |
这包化肥至少含多少千克氮元素? | 31 |
32 | 33 |
我还想深入探究的问题是 34 。
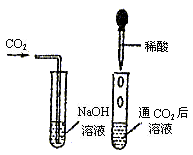
40. 化学复习课上,老师将![]() 分别通入澄清石灰水和
分别通入澄清石灰水和![]() 溶液中,我们观察到前者变浑浊,后者无明显现象。
溶液中,我们观察到前者变浑浊,后者无明显现象。![]() 和
和![]() 是否确实发生了化学反应?
是否确实发生了化学反应?
(1)我设计了甲、乙两个实验装置来验证,如下图所示,实验现象为:甲::软塑料瓶变瘪,乙::“瓶吞鸡蛋”。
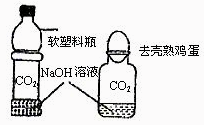
甲 乙
小虎同学认为上述实验是可行的,其共同原理是 35 。
小余同学提出了质疑,他认为上述实验还不足以证明![]() 与
与![]() 确实发生了反应,其理由是 36 。
确实发生了反应,其理由是 36 。
(2)小余同学认为可利用与上述实验不同的原理,设计如下实验方案,我来帮他完成:
| 实验步骤和方法 | 实验现象 | 实验结论 |
方案1 |
| 37 |
|
方案2 | 38 | 39 | 40 |
写出方案2中所涉及的化学方程式 41 、 42 。
四. 我会计算
41. 甲醇(![]() )是一种有毒、有酒的气味的可燃性液体。甲醇在氧气中不完全燃烧可发生如下反应:
)是一种有毒、有酒的气味的可燃性液体。甲醇在氧气中不完全燃烧可发生如下反应:![]() 。若反应生成
。若反应生成![]() 水,
水,
(1)m值是__________。
(2)计算参加反应的氧气的质量是多少克?
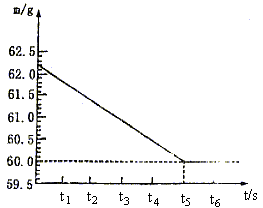
42. 将碳酸钠和硫酸钠的固体混合物6g放入烧杯中(烧杯质量为20g),再加入36.2g稀硫酸,在一定时间内恰好完全反应,无固体剩余。反应时间(t)和烧杯及其所盛物质的总质量(m)的关系如下图所示:
请计算:(1)生成气体的质量为多少克?
(2)求所得溶液中溶质的质量分数是多少?
2018年吕梁中考化学复习题参考答案
一. 选择题:(每小题各1分)
1. A 2. B 3. D 4. B 5. C
6. A 7. D 8. C 9. C 10. B
11. C 12. D 13. D 14. B 15. B
16. B 17. C 18. A 19. B 20. D
21. B 22. D 23. C 24. A 25. C
26. C 27. C 28. C 29. C 30. C
二. 我会填空:(各1分)
31. 1. 蛋白质
32. 2. 3 3. 180 4. 430 5. 0.5
33. 6. ![]() 7. 置换反应
7. 置换反应
34. 8. +1 9. ![]() 遇水蒸气形成盐酸液滴(或盐酸酸雾)
遇水蒸气形成盐酸液滴(或盐酸酸雾)
10. 吸附毒气 11. 石灰水(或氢氧化钙溶液)
35. 12. ![]() (或
(或![]() )
)
13. 用带火星的木条伸入试管中
14. 如果木条复燃,证明所生成的气体是![]() 。
。
(其它答案只要合理即可)
15. ![]() (或
(或![]() )
)
(或![]() )
)
16. B 17. ![]() :C或E;(
:C或E;(![]() :E
:E ![]() :D或C)
:D或C)
18. ![]() :
:![]() (
(![]() :a;
:a;![]() :b)
:b)
19. ![]() (或
(或![]() )
)
36. 20. ![]()
37. 21. 溶 22. ![]()
23. ![]()
24. 不能,因为生成物中无沉淀
25. ![]() (
(![]() )
)
38. 26. 都和![]() 反应 27. 都是化合反应
反应 27. 都是化合反应
28. ![]()
29. 反应③生成的物质是金属氧化物
30. 都生成氧化物
(只要答案合理即可)
39. 31. ![]()
32. 小雨伞图标表示什么?
33. 碳铵保存时要防潮、防雨、防暴晒。
34. 这袋化肥含![]() 的质量是多少千克?
的质量是多少千克?
(32:34空,其它答案只要合理即可)
40. 35. 瓶内![]() 被吸收,产生压强差
被吸收,产生压强差
36. ![]() 与水能反应,生成
与水能反应,生成![]()
37. 有气泡生成
38. 取反应后的溶液少量于试管中,滴加![]() 溶液
溶液
39. 有白色沉淀生成
40. ![]() 和
和![]() 确实发生了化学反应
确实发生了化学反应
41. ![]()
42. ![]()
四. 我会计算:
41. (1)6
(2)设需![]() 质量为x
质量为x
![]()
352 288
x 3.6g
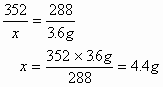
答:略。
42. 解:
(1)2.2g
(2)设混合物中![]() 的质量为x,生成
的质量为x,生成![]() 质量为y
质量为y
![]()
106 142 44
x y 2.2g
![]()
![]()
原混合物中![]() 质量
质量![]()
![]() 溶质的质量分数
溶质的质量分数![]()
答:略。