请选择
由于格式问题此试题可能会出现乱码的情况
为了方便您阅读请点击右上角的全屏查看
2018乐山市中考化学冲刺试题
一、选择题
1. 下列物质的用途只应用其物理性质的是
A. 干冰在舞台制雾时作致冷剂 B.镁粉可作烟花爆竹
C.还原铁粉在月饼盒内作除氧剂 D.生石灰在某些食品袋内作干燥剂
2.在H2O、OH一、H、H+ 四种微粒中,属于分子的是
A.OH一 B.H C.H2O D.H+
3.根据下列微粒的结构,其中属于阳离子的是

4. 水的污染主要来自下列①一⑤中的: ①天然水与空气、岩石和土壤长期接触;②工业生产中废气、废液、废渣的任意排放;③水生动物的繁殖;④城市生活污水的大量排放;⑤农业生产中农药、化肥使用不当。
A.④⑤ B.②④⑤ C.①②③ D.②③④⑤
5. 根据你的生活经验,下列做法不正确的是
A.炒菜时油锅不慎着火,迅速盖上锅盖 B.运动出汗之后,可适当饮用食盐水
C.用燃着的火柴棒检查液化气钢瓶是否漏气 D.做馒头时,可适当加入一些纯碱
6.括号内是区别下列各组常见物质的方法,其中错误的是
A.面粉和葡萄糖(加水,振荡) B.硬水与软水(加肥皂水,振荡)
C.蒸馏水与盐水(过滤) D.白酒和食醋(闻气味)
7.(乐山市中考化学)生活中处处有化学。请根据你所学的化学知识判断下列做法中错误的是
A.用食醋除水壶中的水垢 B.污水厂加明矾作为净水剂
C.用稀硫酸除铁锈 D.在铁桶内配制农药波尔多液
8.下列有关营养成分与人体健康关系叙述错误的是
A.缺铁会患贫血症 B.纤维素不属于糖类
C.摄入淀粉量不足,会患低血糖 D.食用蔬菜、水果可以补充维生素
9.实验室制取下列气体:①用锌和稀硫酸制取氢气;②用双氧水和二氧化锰制取氧气;
③用石灰石和稀盐酸制取二氧化碳气体。下列有关说法错误的是
A.都不需要对气体发生装置加热 B.都不能用排水法收集气体
C.都可用向上排空气法收集气体 D.都可以用相同的发生装置
10. 下列与人的生理活动有关的叙述中不正确的是:
A. 脂肪(由碳、氢、氧元素组成)在人体内代谢的最终产物是二氧化碳和水
B. 剧烈运动时,人体代谢加快,代谢产物不能及时排出,血液pH增大
C. 人的胃液里含有盐酸,可以帮助消化
D. 煤气中毒主要是一氧化碳与血红蛋白牢固结合,使血红蛋白失去输氧能力
11.下列各组物质不发生化学反应的是
A.Fe(OH)3、稀H2SO4 B.NaCI、KOH
C.Fe、 Cu(NO3)2溶液 D.AgNO3、KCI溶液
12.现用质量分数为98%的浓硫酸(密度是1.84g·cm- 3)配制560g质量分数为14%的稀硫酸时,下列有关叙述正确的是
A.配制稀硫酸时,用到的玻璃仪器只需量筒和烧杯
B.配制稀硫酸时,用天平称量所需浓硫酸的质量
C.将80克硫酸倾倒入盛有80 mL98%浓硫酸的500 mL量筒中,并不断搅拌
D.将43.5mL 98%的浓硫酸沿1000mL烧杯内壁缓缓倒入481.6 mL水中,并不断搅拌
13. 乐山市场销售的“桥牌”加碘精制盐中的碘元素是以碘酸根(IO3-)的形式存在。已知在酸性条件下,IO3- 离子能跟碘离子(I-)发生反应生成碘(I2),I2能使淀粉变蓝色。现提供下列试剂和生活中常见的物质:①碘化钾溶液(KI=K++I-) ②食醋 ③食糖 ④白酒 ⑤淀粉 ⑥纯碱,通过实验要证明加碘食盐中存在IO3-离子,必须选用的试剂和物质是
A.①⑤⑥ B.①②③ C.①②⑤ D.②④⑥
14.下图是氢氧化钙的溶解度曲线图。现有10℃含l00 g水的澄清氢氧化钙饱和溶液。
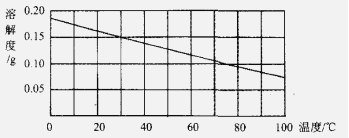
若把该溶液用水浴加热到60℃(水的蒸发忽略不汁).下列说法错误的是
A.溶液变浑浊 B.溶液变为不饱和
C.溶液仍饱和 D.溶质质量分数变小
二、填空题(本大题包含4各小题,每空1分,共计16分)
15.(3分)世界是物质的.物质义是多样的。从下列物质A.陶瓷 B.蛋白质 C.石灰石 D.金刚石 E.纯碱 F.煤炭 G.氨水 H.硝酸铵中,请选择恰当的物质的番号填空。
(1)由原子直接构成的物质 ▲
(2)人体需要的营养物质 ▲
(3)溶于水后会使溶液温度明显降低的物质 ▲
16.(4分)形态各异的物质可按一定规律分类。现有A.石墨 B.二氧化锰 C.氢氧化钾 D.硝酸钾 E.海水 F.硫酸 G.氢氧化铜七种物质,请用相应物质的化学式填空。
(1)属于非金属单质的是 ▲ ;(2)属于易溶性盐的是 ▲ ;
(3)属于易溶性碱的是 ▲ ;(4)属于不挥发性酸的是 ▲ 。
17.(3分)通过钝化的方式使锌制品表面形成一层保护膜,可有效防止锌的腐蚀。某锌制品的钝化液含有硝酸银、硝酸铜、重铬酸等,其中重铬酸是一种可溶性的酸。
(1)该钝化液pH ▲ 7。(填“>”、“<”或“=”)
(2)重铬酸(H2Cr2O7)中铬元素的化合价为 ▲ 。
(3)反应过程中会产生含有金属单质的细微颗粒,该颗粒中一定含有的金属是 ▲ 。
18.(6分)小彤的一副眼镜戴了一段时间后,发现铜质镜架上出现了一墨绿色物质,他想将其除掉。经查阅资料得知:铜在一定条件下会锈蚀生成一种绿色物质,其主要成分是碱式碳酸铜(俗称铜绿)[ Cu2(OH)2CO3],于是他和几个同学按如下方案进行了实验。
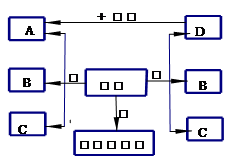
试填空
(1)实验①是向铜绿中加入适量常见无色液体B,再加热至沸,沉淀仍然不变色。实验②、③中C是一种常见的无色气体,B是无色液体。实验③在加热的情况下生成黑色粉末D. 则D的化学式 ▲ A的化学式 ▲
(2)写出实验③反应的化学方程式 ▲
(3)将A的溶液5~9滴滴入5mL10%的氢氧化钠溶液中得到蓝色絮状沉淀,写出其化学反应方程式 ▲ 。蓝色絮状沉淀稍加热即生成黑色沉淀D和无色液体B。写出蓝色絮状沉淀转变为D的化学方程式 ▲ 。
(4)已知2Ca(HCO3) ![]() CaCO3↓+ H2O+CO2↑,则热稳定性CaCO3> Ca(HCO3),由此推理上述实验中铜绿、蓝色絮状沉淀、物质D三种化合物热稳定性由强至弱的顺序是:
CaCO3↓+ H2O+CO2↑,则热稳定性CaCO3> Ca(HCO3),由此推理上述实验中铜绿、蓝色絮状沉淀、物质D三种化合物热稳定性由强至弱的顺序是:
▲ > ▲ > ▲ 。
三、实验探究题 (每空1分,共11分)
19. 某化学兴趣小组利朋下图所示装置进行O 2、CO 2的实验室制法和有关性质的研究。

(1)写出图中编号仪器的名称: ② ▲ 。
(2)甲同学使用A装置用KMnO4固体制取O2,该反应的化学方程式是 ▲ 。
(3)乙同学用稀盐酸和大理石在B装置中反应。长颈漏斗 ▲ 。
(4)丙同学用C装置制取一瓶无色无味的气体(纯净物),你推测该气体可能是 ▲ ,试用最简便的方法证实你的推测 ▲ 。
20. 南南同学跟妈妈学烧紫甘蓝(紫卷心菜),用油妙后加入食醋.发现紫色的叶片立即变红,激发了他的探究欲望。
[提出问题]紫甘蓝的汁液能作酸碱指示剂吗?
[进行实验] 取紫甘蓝叶片少许在研钵中捣烂.用少量水浸泡.滤出蓝紫色的汁液。将汁液分别滴人下列液体中,观察其显示的颜色并记录。
液体名称 | 白醋 | 蒸馏水 | 食盐溶液 | 肥皂水 | 碱溶液 |
紫甘蓝汁液显示的颜色 | 红色 | 蓝紫色 | 蓝紫色 | 蓝色 | 绿色 |
[得出结论l ]紫甘蓝的汁液 ▲ (选填“能”或“不能”)作酸碱指示剂.
[质疑并求证] 紫甘蓝的汁液在均为碱性的肥皂水和纯碱溶液中,为何足示不同颜色?
PH | 7~9 | 10~11 | 12~14 |
紫甘蓝汁液显示的颜色 | 蓝色 | 绿色 | 黄色 |
用pH 试纸测得上述肥皂水和纯碱溶液的pH 分别为9 和11 ,则肥皂水的碱性比纯碱溶液的碱性(选填“强”或“弱”) ▲ 。
查阅资料:
[得出结论2]紫甘蓝的汁液在不同pH 范围内显示的颜色不同,利用紫甘蓝的汁液还可以区分液体碱性的 ▲
[拓展应用] 柠檬酸是制汽水的原料之一,为探究其固休是否显酸性,南南同学联想到教材上 二氧化碳相关实验的设计,准备了三朵用紫甘蓝的汁液染成蓝紫色的干燥小花。
取干燥的花①和喷上水的花②,分别放人盛满二氧化碳的两个集气瓶中。发现花①不变色,花②变成了红色。在干燥的花③上直接撒少最柠檬酸固体花不变色,说明了 ▲ ;再向该花喷水,蓝紫色的花上出现了红色。
[反思]上述花的变色均与水有关,水的作用分别是:
花②中 ▲ ;
花③中 ▲ 。
三、(乐山市中考化学)计算题:(8分)
21.在四个烧杯中都放入Na2CO3和NaCl固体混合物24.8g,分别加入盐酸进行四次实验,所加盐酸和反应后溶液的质量如下表所示:
(1)四个实验中完全反应的是
(2)计算完全反应的实验中所得溶液中溶质的质量分数(CO2的溶解忽略不计)。
实验序数 | 实验一 | 实验二 | 实验三 | 实验四 |
所加盐酸的质量 | 316g | 326g | 336g | 346g |
反应后溶液的质量 | 334.5g | 342g | 352g | 362g |
乐山市中考化学参考答案
选择题:(每题2.5分,共35分。每题只有一个选项符合题意。)
1-14.ACDBC CDBCB BDCB
二、选填题(本题包括4题,每空1分,共16分)
15. (1) D (2)B (3) H
16. (1) C (2) KNO3 (3) KOH (4) H2SO4
17. (1)< (小于) (2) +6 (4)Ag(银)
18.(1)D是CuO A是CuCl2
(2)Cu2(OH)2CO3 ![]() 2CuO + CO2↑ +H2O
2CuO + CO2↑ +H2O
(3) CuCl2 + 2NaOH === Cu(OH)2↓ + 2NaCl Cu(OH)2![]() CuO + H2O
CuO + H2O
(4) D > 铜绿 >氢氧化铜 (氧化铜 > 铜绿 > 氢氧化铜)
三、实验探究题:(本题含2个11分)
19. (1) 锥形瓶
(2) 2 KMnO4![]() K2MnO4 + MnO2 + O2↑ (3)插入液面(伸入液面)
K2MnO4 + MnO2 + O2↑ (3)插入液面(伸入液面)
(4) O2 、用带火星的木条 (CO2、用澄清的石灰水)
20. [得出结论1] 能
[质疑并求证]弱
[得出结论2 ]相对强弱
[拓展应用] 柠檬酸固体不显酸性
[反思] 水与二氧化碳反应生成碳酸,碳酸在水中会解离出H + (碳酸显酸性)
柠檬酸溶解于水,在水中会解离出H + (柠檬酸溶液显酸性)
四、计算题(8分)
21. (1)完全反应的是:实验二---------------------------------------------(1)
(2)解:反应生成的CO2质量=24.8g+326g-342g=8.8g--------------(1分)
设Na2CO3的质量为x,生成的NaCl的质量为y。
Na2CO3+2HCl=2NaCl+H2O+CO2↑------------------------------------------(1分)
106 117 44
x y 8.8g ------------------------------------(1分)
x=21.2g --------------------------------------------(1分)
y=23.4g ------------------------------------------------(1分)
所得溶液中溶质的质量分数=![]() ×100% ≈ 7.9% ---(2
×100% ≈ 7.9% ---(2
(或:所得溶液中溶质的质量分数=![]() ×100% ≈ 7.9% -(2分)
×100% ≈ 7.9% -(2分)
答:所得溶液中溶质的质量分数为7.9%。