请选择
![]() 2018年济南中考化学冲刺试卷【精选word版 】
2018年济南中考化学冲刺试卷【精选word版 】
由于格式问题,部分试题会存在乱码的现象,请考生点击全屏查看!
相对原子质量:H 1 ![]() C
C![]() 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32 Cl 35.5
12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32 Cl 35.5
K 39 Ca 40 Mn 55 Fe 56 Cu 64 Zn 65 Se 79 Ag 108 Ba l37
第Ⅰ卷(选择题共 50分)
一、单项选择题(本大题包括15小题,1-10每小题 3分,11-15每小题4分,共50分。每小题给出的四个选项中,只有一个选项最符合题目的要求)
1.物质世界充满了变化。下列过程中没有发生化学变化的是

A.焚烧秸秆 B.葡萄酿酒 C.冰块融化 D.酸雨腐蚀文物
2.保护碧水蓝天,共享美丽泉城。下列做法,错误的是
A.短距离出行骑共享单车,绿色低碳
B.大力发展露天烧烤,丰富饮食文化
C.市区禁放烟花爆竹,文明过春节
D.回收废旧电池,减少重金属污染
3.每年的4月15日是我国“ 全民国家安全教育日”。下列做法错误的是
A.高层楼房着火时,不能乘坐电梯逃离
B.在加油站张贴严禁烟火的标志
C.进入![]() 久未开启的地窖,要做灯火实验
久未开启的地窖,要做灯火实验
D.在房间里放盆石灰水防止煤气中毒
4.化学是一门以实验为基础的自然学科。下列实验操作中,正确的是
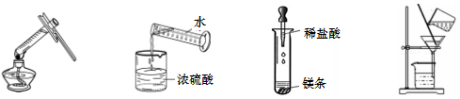
A.加热液体 B.稀释浓硫酸 C.滴加稀盐酸 D.过滤
5.化学与![]() 我们的健康、生活息息相关。下列关于生活常识的说法中,正确的是
我们的健康、生活息息相关。下列关于生活常识的说法中,正确的是
①焙制糕点用小苏打作发酵粉
②香烟的过滤嘴可滤除CO等有害物质,故吸烟对身体无害
③摄入过多量重金属盐会使人中毒
④食用霉变食品可使人引发肿瘤等恶性疾病
A.只有② B.只有①②③ C.只有①③④ D.只有①④
6.用分子的观点解释下列现象,不合理的是
A.酒精挥发——分子消失了 B.气体膨胀——分子间隔变大
C.桂花飘香——分子在不断地运动 D.食物变质——分子本身发生变化
7.根据下图有关信息判断,下列说法中,错误的是
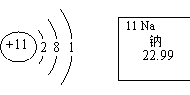
A.钠元素属于金属元素
B.在化合物中,钠元素常显+1价
C.钠元素的原子核外有11个电子
D.钠元素的相对原子质量为22.99克
8.下列说法中,不正确的是
A.自然界中二氧化碳的循环平衡,对地球生命具有重要意义
B.将钢铁制品表面涂保护层是有效减缓钢铁制品锈蚀的方法之一
C.碱溶液中都含有氢氧根离子,因此碱具有相似的化学性质
D.氧化物中都含有氧元素,因此含氧元素的化合物都是氧化物
9.交警常用“酒精检测仪”来检查司机是否饮酒,其检测原理是让司机呼出气体中的酒精与检测仪中的物质发生化学反应:C2H5OH +xCrO3+6H2SO4= 2Cr2 (SO4)3+2CO2↑+9H2O,其中x的值和三氧化铬(C![]() rO3)中铬元素的化合价分别是
rO3)中铬元素的化合价分别是
A.4,+6价 B. 4,+3价C.2,+6价D.2,+3价
10.某化学反应的微观过程可以用下图表示,则下列说法中,正确的是
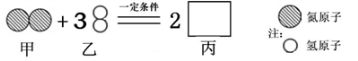
A.该反应中原子的种类发生了改变 B.物质丙的化学式是NH3
C.甲、乙两物质参加反应的质量比为1:3 D.图示反应属于分解反![]() 应
应
11.有一物质X,分成等量的三份,分别加入到足量的NaOH溶液、氯化钡溶液、HCl溶液中,产生的现象如下表。则该物质X是下列各项中的
加入物质 | 氯化钡溶液 | NaOH溶液 | HCl溶液 |
现象 | 产生白色沉淀 | 产生蓝色沉淀 | 无明显现象 |
A.CuSO4溶液 B.(NH4)2CO3粉末 C.稀硫酸 D.CuO固体
12.某同学想用实![]() 验证明CuSO4溶液显蓝色不是由SO42-造成的,下列实验操作中,无意义的是
验证明CuSO4溶液显蓝色不是由SO42-造成的,下列实验操作中,无意义的是
A.观察Na2SO4溶液,溶液没有颜色
B.向CuSO4溶液中滴加足量氯化钡溶液,充分反应后,溶液颜色未消失
C. 对比不同浓度的CuSO4溶液的颜色差异,浓度小的溶液颜色较浅
D. 向CuSO4溶液中滴加足量氢氧化钠溶液,充分反应后,溶液颜色消失
13.除去下列物质中混有的少量杂质,所用试剂和操作方法均正确的是
序号 | 物质 | 杂质 | 所用试剂和操作方法 |
A | H2气体 | HCl | 通过足量的AgNO3溶液,干燥 |
B | Na2CO3溶液 | Na2SO4 | 加入过量的Ba(NO3)2溶液,过滤 |
C | CO2气体 | HCl | 通过足量的NaOH溶液,干燥 |
D | 铁粉 | Fe2O3 | 加入过量的稀盐酸,过滤 |
14.含有AgNO3、Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后,过滤,向滤液中滴入NaCl溶液,有白色沉淀产生。则下列对滤渣成分的判断中,正确的是
A. 只有Fe B. 只有Ag C. 只有Zn和Ag D. 只有Fe和Ag
15.现有14.2g Mg(OH)2与MgCO3的固体混合物,其中镁元素与碳元素![]() 质量比为4:1。在
质量比为4:1。在![]() 室温下,将该混合物与100g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为109.8g,则原固体混合物中含有镁元素的质量为下列的
室温下,将该混合物与100g稀硫酸混合,恰好完全反应,所得不饱和溶液的质量为109.8g,则原固体混合物中含有镁元素的质量为下列的
A.9.6g B.4.8g C.2.4g D.1.2g
第Ⅱ卷(非选择题共 50分)
二、非选择题(本大题共 6 小题,共 50 分)
16.(5分)按要求从二氧化碳、氧气、氯化钠、碳酸钠、氢氧化钙、盐酸中选择合适的物质,将其化学式填写在下列横线上。
(1)能供给呼吸的气体单质____________ (2)可用于人工降雨的氧化物____________
(3)胃酸的主要成分__________________ (4)常用来腌渍食品的盐________________
(5)用来中和酸性土壤的碱____________
17.(5分)香烟燃烧产生的烟雾中主要含有一氧化碳、尼古丁和焦油,这三种物质被称为香烟的三大杀手。试回答下列问题:
(1)在一氧化碳、尼古丁这两种物质中,属于氧化物的是____________。
(2)尼古丁的化学式为C10H14N2,该物质的每一个分子中共含________个原子。
(3)尼古丁中,碳、氢两元素的质![]() 量之比为_____________(填最简整数比)。
量之比为_____________(填最简整数比)。
(4)尼古丁中,所含元素的质量分数最大的元素是___________。
(5)下列说法中,错误的是_________(填写下列各项的序号)。
①公共场所吸烟不影响他人健康②焦油能诱发细胞癌变
③生活中应远离有毒物质④吸烟会产生依赖性
18.(10分)工业上采用氨碱法生产纯碱(Na2CO3),主要流程如图1:
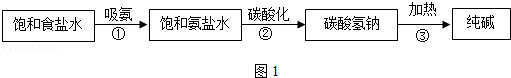
(1)在①〜③三个过程中,发生分解反应的是____________(填序号)
(2)侯氏制碱法以食盐为主要原料制取纯碱,制得的纯碱中常含
有少量氯化钠。Na2CO3和NaCl的溶解度曲线如图2所示,
试回答下列问题:
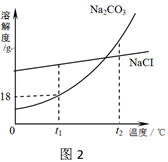
①在t1℃时,Na2CO3的溶解度是 g
②t2℃时,NaCl的溶解度_______Na2CO3的溶解度(填“大于”“等
于”“小于”之一)
③要从海水中提取NaCl,应采用的方法是_________________
(填“蒸发结晶”或“降温结晶”)
④若把10g的Na2CO3加入50g水中,充分溶解后,得到t1℃的Na2CO3溶液的质量是
g
19.(10分)下图所示为实验室中常见的气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器)。试根据题目要求,回答下列问题:

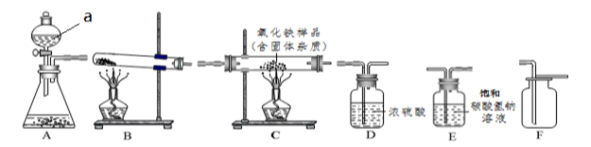
(1)若以石灰石和稀盐酸为原料制取二氧化碳,因盐酸会挥发出少量的氯化氢气体,导致制取的气体不纯,可用饱和碳酸氢钠溶液吸收。现要制备、收集一瓶干燥的、不含氯化氢的二氧化碳气体。①所选仪器的连接顺序为__________________________(填写仪器序号字母)
②仪器a![]() 的名称是_________________
的名称是_________________
③生成二氧化碳时,A中所发生反应的化学方程式为______________________________
④将少量的CO2气体通入盛有大量澄清Ca(OH)2溶液的大烧杯中,烧杯中溶液的质量与之前相比会__________ (填“增大”“减小”“不变”之一)。
(2)小强同学欲用一氧化碳气体测定某不纯氧化铁样品的纯度(杂质不参与任何反应),小强同学取2.5g氧化铁样品设计了实验方案:气体流向是从左向右,选择的仪器按“一氧化碳气体→C→尾气处理装置”顺序连接,然后进行实验(假设有关反应均反应完全)。若其他操作正确,反应结束后测得C装置减少了0.48g(不考虑空气中成分对装![]() 置质量的影响),则此氧化
置质量的影响),则此氧化![]() 铁样品中氧化铁的质量分数为______________。
铁样品中氧化铁的质量分数为______________。
20.(10分)有一固体混合物A,已知其中可能含有MgCl2、CuSO4、CaCO3、FeCl3四种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(假设过程中所有发生的反应都恰好完全进行)。
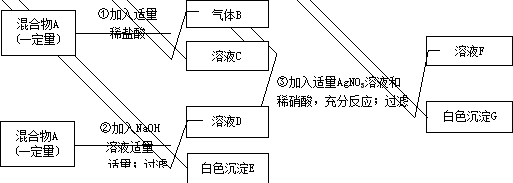
![]() 试根据实验过程和发生的现象做出判断,填写以下空白:
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)气体B的化学式为________________
(2)在混合物A里,上述四物质中肯定不存在的物质是______________________(写化学式)
(3)在溶液F中,主要含有_________种溶质,其中大量含有的酸根离子符号是_____________
(4)写出1个生成白色沉淀G的化学方程式:__________________________________________
21.(10分)某化学小组的同学对金属元素及金属材料进行系列研究。
(1)“越王勾践剑”埋藏在地下两千多年,出土时依然光彩夺目、锋利无比,几乎没有丝毫锈蚀。下列选项中,与其保存完好的原因无关的是___![]() ________________(填序号)
________________(填序号)
A.埋藏环境中的氧气少 B.剑身曾经过防锈表面处理
C.材料(青铜)本身不容易生锈 D.埋藏环境的压强比较恒定
![]()
![]() (2)我们的祖先很早就掌握了用孔雀石(主要成分是Cu2(OH)2CO3)和木炭一起加热进行火法炼铜的工艺。有关化
(2)我们的祖先很早就掌握了用孔雀石(主要成分是Cu2(OH)2CO3)和木炭一起加热进行火法炼铜的工艺。有关化![]() 学反应是:① Cu2(OH)2CO3==2CuO+ CO2↑+ H2O ②2CuO+ C=== 2Cu + CO2↑。上述反应②属于________________类型。(选填“置换反应”、“复分解反应”之一)
学反应是:① Cu2(OH)2CO3==2CuO+ CO2↑+ H2O ②2CuO+ C=== 2Cu + CO2↑。上述反应②属于________________类型。(选填“置换反应”、“复分解反应”之一)
(3)碱式碳酸铜【化学式是Cu2(OH)2CO3】是一种不溶于水的固体粉末,取一定量该固体,放入干净的烧杯中,逐渐滴入溶质质量分数为10%的稀硫酸,滴入该稀硫酸的质量和反应产生气体的质量关系曲线如图所示。
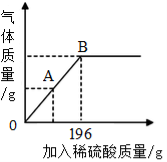
【已知:Cu2(OH)2CO3+2H2SO4=2CuSO4+CO2↑+3H2O】
请回答下列问题:
①当滴入上述稀硫酸至图中A点时,烧杯内溶液中大量存在
的溶质为 (填写化学式)
②当滴入上述稀硫酸至图中B点时,试通过计算,求此时所得不饱和溶液中溶质的质量。
![]() 2018年济南中考化学冲刺试卷参考答案
2018年济南中考化学冲刺试卷参考答案
一、单项选择题(本大题包括15个小题,1-10题每小题3分,11-15题每小题4分,共50分。)
1.C 2.B 3.D 4. D 5.C 6.A 7.D 8.D 9.A 10.B 11.A 12.C 13.A ![]() 14.B 15.B
14.B 15.B
二、非选择题(本大题包括6个小题,共50分)
16.(5分,每空1分)(1)O2(2)CO2(3)HCl (4)NaCl (5) Ca(OH)2
17.(5分,每空1分) (1)CO(一氧化碳) (2)26 (3)60:7 (4)C(碳) (5)①
18. (10分,每空2分) (1)③ (2)18 小于 蒸发结晶 59
19. (10分,每空2分)(1) A-E-D-F 分液漏斗 CaCO3+2HC1=CaCl2+H2O+CO2↑ 减小 (2) 64%
20.(10分,每空2分)(1)CO2; (2)CuSO4 FeCl3 (3)4 NO3-
(4)NaCl + AgNO3=AgCl↓+ Na NO3(其它合理答案可给分)
21.(10分)(1)D (2)置换反应 (3)①CuSO4
②解:设CuSO4的质量为x
196g x10%=19.6g ……………………………1分
Cu2(OH)2CO3 + 2H2SO4 = 2CuSO4 + CO2↑ + 3H2O ……………………………1分
196 320
19.6 g x

x=32g ……………………………………………2分
答:此时所得不饱和溶液中溶质的质量为32g。