请选择
![]() 德阳市2018年初中毕业生学业考试与高中阶段学校招生考试
德阳市2018年初中毕业生学业考试与高中阶段学校招生考试
理科综合试卷(化学部分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Ca-40 Fe-56 Cu-64 Ag-108
选择题(本体共8小题,每小题3分,共24分)
古丝绸之路贸易中的下列商品,主要成分属于无机化合物的是( )
丝绸 B.草药 C.茶叶 D.瓷器
下列图示的实验操作中,正确的是( )
A B C D
3.丁烯(C4H8)是一种重要的化工原料,下列有关说法正确的是( )
A.丁烯中碳氢元素质量比为1:2
B.丁烯中的碳元素位于元素周期表中的第二周期
C.丁烯分子中碳原子原子结构示意图为
D.丁烯分子中有4个碳元素和8个氢元素
4.如图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子.你认为下列说法正确的是( )![]()
A. 该反应属于化合反应 B. 反应前后原子的种类和数目不变
C. 生成物一定是氧化物 D. 反应前后各元素的化合价发生了变化
5.下列鉴别两种不同的物质的方法,错误的是( )
选项 | 待鉴别的物质 | 鉴别方法 |
A | CO2与O2 | 燃着的木条,观察木条燃烧情况 |
B | 棉线与羊毛绒 | 点燃,闻产生的气味,观察生成的灰烬 |
C | AgCl与NaCl | 加水,观察是否溶解 |
D | NaOH与Na2CO3 | 溶于水,滴加酚酞试液,观察溶液的颜色变化 |
如图是甲、乙两种固体物质的溶解度曲线,下列说法中正确的是( )
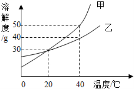
A. 20℃时,甲、乙的饱和溶液溶质质量分数相等
B. 40℃时,甲的溶解度大于乙的溶解度
C. 40℃时,乙的饱和溶液中溶质的质量分数为40%
D. 将40℃甲的饱和溶液降温到20℃,会有晶体析出
向一定质量CaCl2和HCl的混合溶液中逐滴加入溶质质量分数为10.6%的Na2CO3溶液。反应过程中加入的Na2CO3溶液的质量与产生沉淀或气体的质量关系如图所示。下列说法错误的是( )
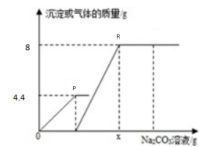
A. P点时的溶液中只含一种溶质
B. R点对应横坐标的数值为180
C. O到P过程中溶液的PH变大
D.Q至R段表示生成沉淀的过程
8.向一定量的硝酸铜和硝酸银中加入5.6g铁粉,充分反应过滤、洗涤、干燥,称得固体14g。向固体中加入稀盐酸,无气泡产生。则下列分析正确的是( )
A.滤液中一定不含硝酸银 B.滤液中一定含有硝酸铜
C.滤出的固体含有银7.6g D.滤出的固体含有铜6.4g
二、填空题(本题包括5个小题,共36分)
9.(6分)防止空气污染、改善生态环境已成为全民共识。近年来,一些城市空气中出现可吸入悬浮颗粒物与雾形成“雾霾”天气。粒径不大于2.5纳米的可吸入悬浮颗粒物(PM2.5)富含大量有毒、有害物质。
(1)下列行为可能会导致“雾霾”加重的是 (填序号)
A.燃煤脱硫 B.植树造林 C.静电除尘 D.燃放鞭炮
(2)为了减少雾霾和降低大气中的有害气体含量,研究机动车尾气中CO、NO、CxHy的排放量意义重大。机动车尾气污染物的含量与“空/燃比”(空气与燃油气的体积比)变化关系如右图所示。
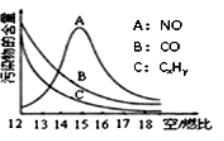
①利用氨气可将汽车尾气的氮氧化合物在一定条件下转化为对空气无污染的物质。请将该反应的化学方程式补充完整:![]()
②随“空/燃比”增大,CO和CXHY的含量减少的原因是 。
(8分)A~F是初中化学的常见物质,A与B的组成元素相同,D、E在通常状况下是气体,F是大理石的主要成分。其转化关系如下图所示,部分反应物、生成物和反应条件未标出.

A的化学式是 。
若B+E+F→C,则C是 。(填名称或化学式)
反应④的化学方程式是 。
反应⑤的化学方程式是 。
11.(8分)氢氧化镁是一种重要的化工原料。某矿石由MgO、Fe2O3、CuO和SiO2组成。
用它制备氢氧化镁的流程示意图如下:
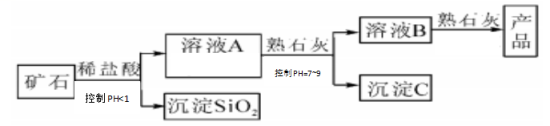
部分金属阳离子以氢氧化物形成沉淀时的溶液的PH见下表:
沉淀物 | Fe(OH)2 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
熟石灰的化学式 ;
溶液A的阳离子是 (填离子符号);
沉淀C的成分是 ;
溶液B与熟石灰反应的化学方程式是 。
12.草酸(乙二酸)存在于自然界的植物中。草酸晶体(H2C2O4⋅2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。草酸能与氢氧化钙反应生成沉淀:![]() 回答下列问题:
回答下列问题:
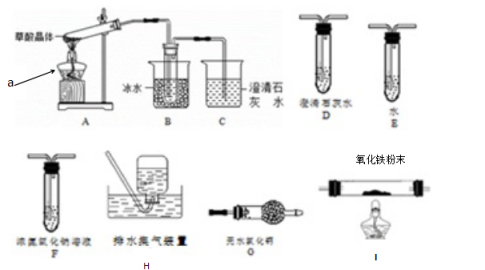
甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。仪器a的名称 装置B的主要作用是 装置C中有气泡逸出,澄清石灰水变浑浊。由此可知草酸晶体分解的产物中有 .
(2)乙组同学认为草酸晶体分解的产物中含有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可以重复选用)进行实验。
①乙组同学的实验装置中,依次连接的合理顺序为A→B→( )→( )→( )→I→D→H。
②装置I中盛有的氧化铁发生了颜色变化,欲证明草酸晶体分解的产物中有CO,乙组同学需要两次使用装置D,其现象分别是
(4分)某工厂利用废硫酸与废铁屑反应制取硫酸亚铁。现取废硫酸4.9t与足量的废铁屑反应,得到![]() 1.52t。计算废硫酸中
1.52t。计算废硫酸中![]() 的质量分数。
的质量分数。