请选择
![]()

3、某无土栽培所需的营养液成分是含有N、P、K、Ca等元素的无机盐,该配方适用于苦瓜、黄瓜、生菜的种植。可作营养液成分的是
A. P2O5 B.KOH C.NH4Cl D. CaCO3
4、规范实验操作是我们完成实验的基本保障,你认为以下操作正确的是

A.稀释浓硫酸 B.倾倒CO2 C.O2验满 D.滴加液体
5、1869年门捷列夫编制了元素周期表。硫元素也排列其中,其化合价分别为-2、0、+4,+6价,依次对应的化学式错误的是
A H2S B.S C.SO2 D. H2SO3
6、色氨酸(C11H12N2O2)是氨基酸中的一种,在人体内含量太低会影响睡眠质量。一般可通过食补黄豆、黑芝麻、海蟹和肉松等得以改善。有关色氨酸的叙述正确的是
A.它的分子内含四种元素 B.它含有氮分子
C.它共含有27个原子 D.其中的碳属于人体所需的常量元素
7、生活中的自来水通常用氯气(Cl2)进行杀菌消毒处理,发生反应的化学方程式是Cl2+ H2O=X+HClO。则X的化学式为
A.H2 B. ClH C.HCl D.ClO2
8、厉害了,我的国!我国航天技术迅猛发展,“天舟一号”与在轨运行的“天宫二号”空间实验室首次成功交会对接,有力推动了我国空间站建设的进程。空间站里的O2源自电解水,所得H2与CO2反应生成H2O和CH4,该反应的微观示意图如下。依据图示,下列叙述错误的是
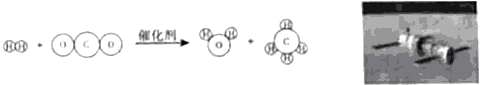
A.反应前后分子种类不变 B. 原子可以构成分子
C.反应中分子可以再分 D.反应前后原子种类不变
9、验证镁、铜的金属活动性顺序,下列试剂不能选用的是
A.MgSO4溶液 B.KCl溶液 C.稀盐酸 D.ZnCl2溶液
10、利用溶解度曲线,可以获得许多有关物质溶解度的信息。下图是a、b两物质的溶解度曲线。有关叙述正确的是
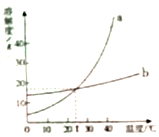
A. a的溶解度大于b的溶解度
B.当a物质中混有少量b物质时,可以用蒸发结晶的方法除去b
C.10℃时,取相同质量的a、b两物质分别配成饱和溶液所需水的质量是a大于b
D.将1℃时a、b的饱和溶液升温至40℃,其溶液中溶质的质量分数为a大于b
可能用到的相对原子质量: H-1 N-14 O-16 Zn-65
三、生活、生产应用题(本大题共5个小题。化学方程式每空2分,其余每空1分,共16分。)
【关注生活现象】
21、能源既是国家经济发展的命脉。也是国家发展战略的重要支柱。我省多地有效调整能源结构,稳步发展安全高效的能源体系,合理利用如下三种发电方式,并取得了显著成效。

(1)与C相比,A、B发电的共同优点是_________________________(写一条)。
(2)A的能量转化方式是把______能经过一系列变化转化成电能。
22、食盐是重要的调味品,其主要成分的化学式是____________。蒸馒头时,既能除去面团中的酸又能使馒头变得松软,可加入小苏打,其化学式是__________________。
23、当你漫步阿根廷的布宜诺斯艾丽斯时,会被这里精美绝伦的雕塑所吸引,“花之魂”就是世界10大奇异雕塑之一(图甲),它是由钢和铝(6% ~16%)加工而成的巨型“花朵”。傍晚时分“花朵”霓虹闪烁,将城市的夜晚打扮得流光溢彩,美轮美奂。

(1)钢铝加工而成的“花之魂”比铁雕塑性能优良之处_________________________(写一条)。
(2)目前金属耗速过快,替代材料越来越多。列举生活中常用的一种合成材料_______________。
(3)图乙是铝的原子结构示意图,铝原子在化学反应中易_________电子(填“得”或“失”)。
24、在山西省人民医院消化科的宣传栏里,有这样一则宣传:

(1)观察图1,集体就餐时,为避免疾病传播应该注意的是_________________________(写一条)。
(2)胶囊中尿素的相对分子质量是______________。农业生产所使用的化肥中,尿素可用作______肥。
【关注生产实际】
25、科学精神与社会责任,是化学学科素养更高售层面的价值追求。在一次实践活动中,小红和同学们一起参观了某钢铁公司。大家对矿石选取,冶铁和炼钢的工艺流程(如图)、生铁和钢的区别等,有了全新的认识。
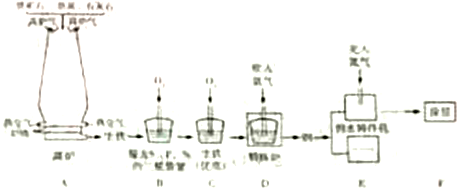
(1)用赤铁矿石冶铁的反应原理是_________________________(用化学方程式表示)。 (2)分析工艺流程,三脱装置中发生反应的化学方程式是_________________________(写一个)。
(3)向精炼炉中吹入氯气使钢水循环流动,各成分均匀混合,相当于化学实验中______________的作用(填一种仪器的名称)。
(4)在钢水铸件机中,高温钢加工成钢制零件时,充入氮气的作用是_______________。
四、科普阅读题(本大题共1个小题。每空1分,共7分。)
26、
 综合分析上述材料,回答下列问题:
综合分析上述材料,回答下列问题:
(1)南海丰富的资源中,油气属于_____________(填“纯净物”或“混合物”)。对石油加热炼制时,根据各成分的________不同可得到的产品有________(写一种)。
(2)天然气可压缩储存于钢瓶中,用分子的观点解释其变化______________-。
(3)材料2中所述锰、镁、铜等是指_____________(填“元素”或“原子”)。
(4)海洋鱼类、海参、龙虾富含的营养素是________________。
(5)南海自古就是中国的!我们要捍卫祖国的领士、领海和资源的完整。在资源的开发利用方面你的一点建议是__________________________________________。
五、物质组成与变化分析题(本大题共1个小题。化学方程式每空2分,其余每空1分,共6分。)
27、思维导图是激发大脑潜能,练就科学思维的有效方法。A-D是初中化学常见的四种物质,A可用于金属除锈,B难溶于水。它们相互之间的关系如图所示,“—”表示两种物质之间可以相互反应,“→”表示一种物质可生成另一种物质。分析推理,回答问题:
(1)A的化学式为_______________。A 与D反应的实质为______________________。
(2)A生成B的化学方程式_______________________________。
(3)C与D反应的化学方程式__________________________。
六、实验探究题(本大题共2个小题。化学方程式每空2分,其余每空1分,共15分。)
28、右图是实验室用高锰酸钾制取氧气的装置。请回答问题。

(1)仪器a的名称______________。
(2)用高锰酸钾制取O2的化学方程式是__________________________________。
(3)实验室收集氧气的方法是__________________________。
(4)将高锰酸钾粉末装入试管的操作是__________________________。
(5)试管口放一团棉花的作用是__________________________。
【科学探究】
29、化学实验过程经常会产生一定量的废液,经过无害化处理可有效防止水体污染。在一次实验课上,兴趣小组的同学们完成了NaOH溶液和Na2CO3溶液的鉴别,并对废液成分展开探究。

活动一
通过小组合作,同学们完成了右图所示的三组小实验。实验中生成白色沉淀的化学方程式是__________________________________(写一个)。
活动二
小雪将六支试管中的剩余物倒入一个洁净的大烧杯中(如下图), 充分搅拌、静置。观察到杯内上层是无色溶液,下层有白色沉淀。由此可以确定:上层溶液中一定不含有的离子是__________________、以及一定含有的离子。小组同学对上层溶液中还可能含有的离子进行了如下探究。
【提出问题】上层溶液中还可能含有什么离子?
【猜想与假设】上层溶液中还可能含有OH-、CO32-、Ca2+中的一种或几种。
【进行实验】
实验步骤 | 实验现象 | 实验结论 | |
方案一 | ①取少量溶液于试管中,滴加无色酚酞溶液②继续滴加稀盐酸 | 溶液变红 ②产生气泡 | ①有OH- ②有CO32-、无Ca2+ |
方案二 | 取少量溶液于试管中,________________(指示剂除外) | ①___________________ ②____________________ | ①有CO32-、无Ca2+ ②有OH- |
【反思与评价】
(1)小明同学对方案一提出质疑, 他的理由是________________________。
(2)经过综合分析,最终确定上层溶液中肯定存在的离子有______________________。
(3)将烧杯内物质过滤,滤渣回收,向滤液中加入适量__________________________ 进行处理后再排放。
七 、定量分析题(本大题共1个小题,共6分)
30、黄铜(铜锌合金)的外观与黄金极为相似、容易以假乱真。小红同学想测定黄铜中锌的含量。她称取20g黄铜样品放入烧杯中,加入足量稀硫酸充分反应后,测得生成氢气的质量为0.2g。
(1)该反应属于____________(填基本反应类型)。
(2)求黄铜样品中锌的质量分数(写计算过程)。

3-10 CBDDC ABC
21、(1)节约资源(或绿色环保/无废渣废气排放)(合理即可) (2)风
22、NaCl NaHCO3
23、(1)耐腐蚀(或不易生锈/硬度大/经久耐用)(合理即可)
(2)塑料(或合成纤维/合成橡胶/聚乙烯)(合理即可)
(3)失
24、(1)用公筷(或分餐制)(合理即可) (2)62 氮
25、(1)3CO+Fe2O3=2Fe+3CO2
(2)S+O2![]() SO2 [或4P+5O2
SO2 [或4P+5O2![]() 2P2O5/Si+O2
2P2O5/Si+O2![]() SiO2(本题的反应条件写成“加热”“高温”“点燃”都得分,未写反应条件扣1分)]。
SiO2(本题的反应条件写成“加热”“高温”“点燃”都得分,未写反应条件扣1分)]。
(3)玻璃棒
(4)做保护气(或隔绝氧气)(合理即可)
26、(1)混合物 沸点 汽油(或柴油石蜡/沥青等)
(2)(压强增大)分子间间隔变小 。
(3)元素 (4)蛋白质
(5)合理开发 (或谨慎开采/有计划开采) (合理即可)
五、物质组成与变化分析题(本大题共1个小题。化学方程式每空2分,其余每空1分,共6分。)
27、(1)HCl(或H2SO4) 氢离子与氢氧根离子生成水分子(或H+与OH-生成H2O分子/H+与OH-生成H2O)。
(2)H2SO4 + BaCl2=BaSO4↓+2HC1 (或HCl +AgNO3=AgC1↓+HNO3 (合理即可)
(3)CO2+Ca(OH)2= CaCO3↓+H2O (或SO2+ 2NaOH=Na2SO3 + H2O) (合理即可)。
六、实验探究题。(本大题共2个小题。化学方程式每空2分,其余每空1分,共15分。)
28、(1)铁架台
(2)2KMnO4![]() K2MnO2+MnO2+O2↑
K2MnO2+MnO2+O2↑
(3)向上排空气法(或排水法)
(4)将试管倾斜(或横放),把盛有药品的药匙(或纸槽)送至试管底部,然后使试管直立起来。
(5)防止加热时高锰像钾粉末进入导管(或防止高猛配钾粉末进入水槽使水变红(合理即可)
【科学探究】
29、活动一 Ca(OH)2+Na2CO3 =CaCO3↓+2NaOH(或CaCl+Na2CO3=CaCO3↓+2NaCl)
活动二 H+(或氢离子)
实验步骤 | 实验现象 | 实验结论 | |
方案一 | ①取少量溶液于试管中,滴加无色酚酞溶液②继续滴加稀盐酸 | 溶液变红 ②产生气泡 | ①有OH- ②有CO32-、无Ca2+ |
方案二 | 取少量溶液于试管中,滴加过量的BaCl2溶液,静置,继续滴加CuSO4溶液,(或滴加过量的Ca(NO3)2溶液,静置,继续滴加FeCl3溶液。(合理即可)(指示剂除外) | ①产生白色沉淀 ②产生蓝色沉淀(或产生红褐色沉淀)(合理即可) | ①有CO32-、无Ca2+ ②有OH- |
(1)溶液中有CO32-(或Na2CO3)也会使酚酞变红,无法判断是否含OH-[或溶液中有CO32-(或Na2CO3)溶液也显碱性,无法判断是否含OH-](合理即可)
(2)Na+、 Cl-、OH-、CO32- (或钠离子、氯离子、氢氧根离子、碳酸根离子)
(3)稀硫酸(或稀盐酸/酸)(合理即可)
30、(1)置换反应(1分)
(2)解:设黄铜样品中锌的质量为x
Zn+H2SO4=ZnSO4+H2↑(1分)
65 2(1分)
x 0.2g (1分)
![]() =
=![]() (1分)
(1分)
x=6.5g(1分)
黄铜中锌的质量分数=![]() ×100%=32.5%(1分)
×100%=32.5%(1分)
答:黄铜中锌的质量分数为32.5%。